近日,化学与分子工程学院罗细亮/徐升豪课题组成功开发出一种基于自催化环状DNA(cir-DNA)的等离子体CRISPR/Cas12a分子诊断平台,通过整合正反馈放大机制与空间限域效应,实现了非核酸生物标志物的超灵敏、快速检测。通过巧妙的分子电路设计与利用纳米等离子体增强策略,攻克了非核酸生物标志物检测中灵敏度不足与反应动力学缓慢两大技术瓶颈。研究成果近期以题为《Autocatalytic Circular DNA Powered Plasmonic CRISPR/Cas12a Platform for Ultrasensitive Non-Nucleic Acid Target Sensing》发表化学领域顶级期刊在Angewandte Chemie International Edition上。
传统CRISPR/Cas12a分子诊断平台在检测非核酸目标(如蛋白质、小分子污染物)时,由于目标物无法像核酸一样进行预扩增,导致灵敏度严重受限。研究团队设计了信号转换器并创新性地引入了一种cir-DNA结构,该结构同时包含可被Cas12a切割的单链区域和能够激活Cas12a的双链区域。当目标物存在时,释放的单链DNA(ssDNA)激活器激活初始的Cas12a活性,随后切割cir-DNA并将其转化为线性双链DNA激活器,新生成的线性双链DNA激活器又能激活更多的Cas12a,形成“激活-切割-再激活”的自催化循环,从而产生级联信号放大效应(图1)。
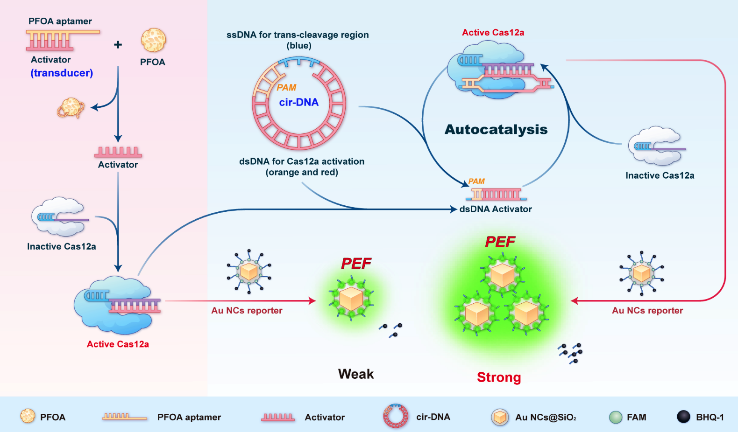
图1 基于正反馈自催化环状DNA的等离子体CRISPR/Cas12a分子诊断平台用于非核酸靶标检测示意图。
针对荧光染料光漂白导致的灵敏度不足问题以及CRISPR/Cas 12a与传统ssDNA报告子之间随机碰撞导致的切割反应动力学速率低、稳定性差等问题,作者合成了金纳米立方体(Au NCs)并选择其作为空间限制效应和PEF基底,制备了Au NCs报告子(图2)。与传统ssDNA报告子相比,Au NCs报告子具有更快的反应动力学,反应时间缩短至15min,荧光强度提高了近7.8倍。此外,由于球形核酸设计,Au NCs报告子对核酸酶(如DNase I)以及FBS的抗降解能力也得到了提升(图3)。
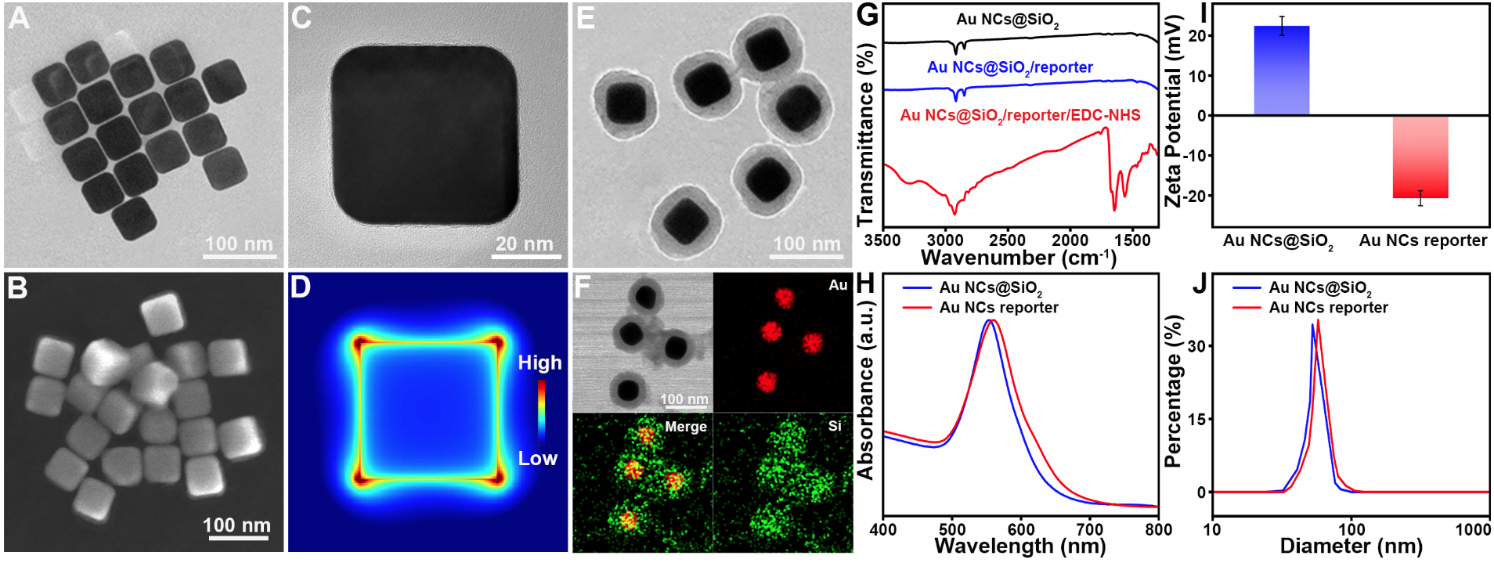
图2 金纳米立方体的透射电镜、扫描电镜等表征以及金纳米立方体报告子的红外光谱、Zata电位、吸收光谱及DLS表征。
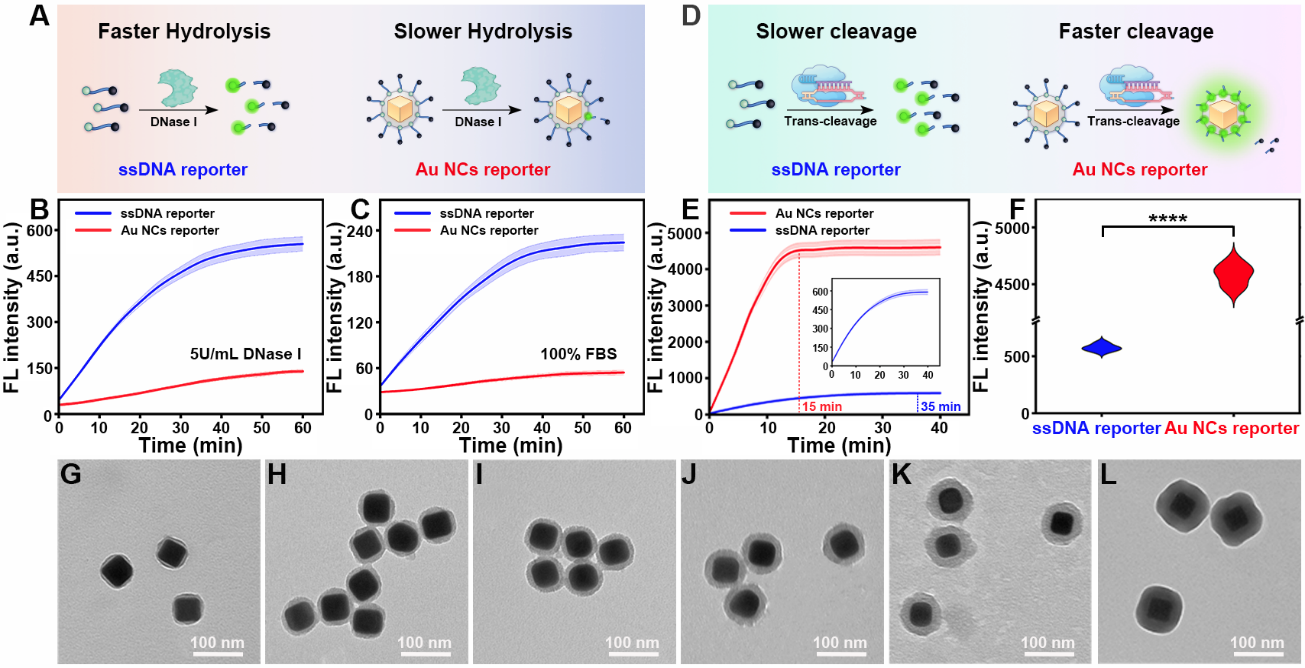
图3 金纳米立方体报告子与传统ssDNA报告子的反应动力学及稳定性对比。
在以环境污染物全氟辛酸(PFOA)为模型的检测中,该分子诊断平台对PFOA的检测灵敏度较传统方法提升了52倍。同时,如图4所示,本研究还引入卷积神经网络(CNN)模型,通过对荧光图像空间特征的提取,实现了对阈值附近样本的精准区分。CNN模型将盲测样本分类准确率AUC值从79.1%提升至97.7%。
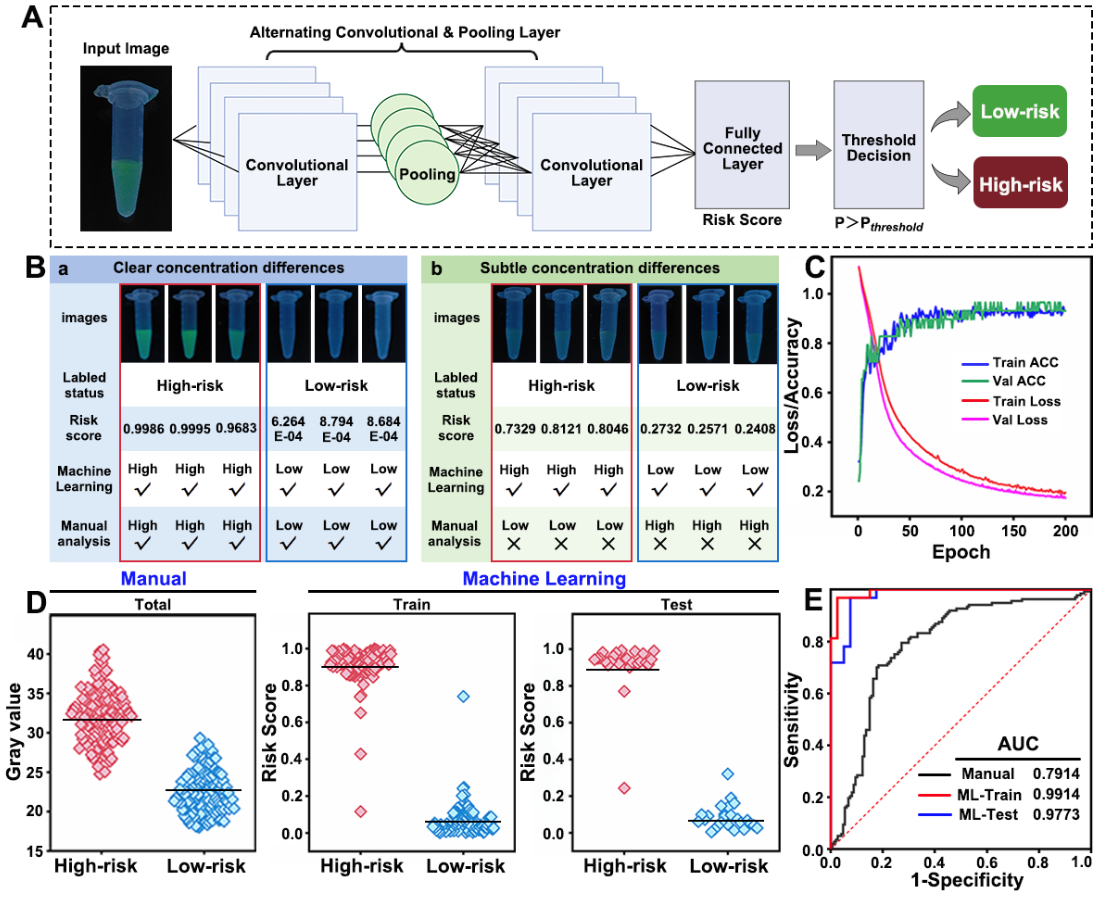
图4 基于CNN的PFOA检测风险分层工作流程及性能分析。
该研究成果首次成功将自催化DNA电路、等离子体增强技术与CRISPR/Cas12a技术深度融合,创建了一个快速、超灵敏的非核酸靶标检测平台,不仅为环境污染物监测提供了新方案,更在妊娠风险评估、疾病早期诊断等领域展现巨大应用潜力。该研究得到国家自然科学基金(21505081、22374085))、山东省自然科学基金面上项目(ZR2023MB110)的资助支持,文章的第一作者是2023级硕士研究生姚旺,通讯作者是罗细亮教授和徐升豪副教授。
论文信息:Wang Yao, Xiaohan Xu, Xingguo Zhai, Tong Ji, Ruyi Zhang, Shenghao Xu, and Xiliang Luo. Autocatalytic Circular DNA Powered Plasmonic CRISPR/Cas12a Platform for Ultrasensitive Non-Nucleic Acid Target Sensing. Angew. Chem. Int. Ed. 2025, DOI: 10.1002/anie.202516838
https://onlinelibrary.wiley.com/doi/10.1002/anie.202516838






